
- English
- Español
- Português
- русский
- Français
- 日本語
- Deutsch
- tiếng Việt
- Italiano
- Nederlands
- ภาษาไทย
- Polski
- 한국어
- Svenska
- magyar
- Malay
- বাংলা ভাষার
- Dansk
- Suomi
- हिन्दी
- Pilipino
- Türkçe
- Gaeilge
- العربية
- Indonesia
- Norsk
- تمل
- český
- ελληνικά
- український
- Javanese
- فارسی
- தமிழ்
- తెలుగు
- नेपाली
- Burmese
- български
- ລາວ
- Latine
- Қазақша
- Euskal
- Azərbaycan
- Slovenský jazyk
- Македонски
- Lietuvos
- Eesti Keel
- Română
- Slovenski
- मराठी
- Srpski језик
Bosutiniib CAS 380843-75-4
2023-08-21
Keemiline nimetus:
4-(2,4-dikloro-5-metoksüanilino)-6-metoksü-7-[3-(4-metüülpiperasiin-1-üül)propoksü]kinoliin-3-karbonitriil
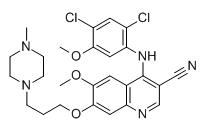
M.F:C26H29Cl2N5O3
Keemilised omadused:Kahvatukollane tahke aine
Bosutiniib on Bcr-Abl kinaasi inhibiitor Philadelphia kromosoompositiivse (Ph+) kroonilise müelogeense leukeemia (CML) raviks. Võrreldes teiste türosiinkinaasi inhibiitoritega on sellel soodsam hematoloogiline toksilisuse profiil. FDA kiitis heaks 4. septembril 2012. aastal.
Uuendaja:Wyeth Pharmaceuticals (Pfizer) (USA)
Rakendused:
Mõju rakumorfoloogiale täheldati kontsentratsioonil 1 uM SKI-606 kõigi uuritud rakuliinide puhul ja morfoloogilised muutused ilmnesid juba 0,25 uM kontsentratsioonidel. SKI-606 pani rakud üksteise külge kleepuma, moodustades võrreldes kandjakontrolliga (DMSO) töödeldud rakkudega tihedaid klastreid, mis näitasid levimist suurematele aladele.
Annustamisvorm: Suukaudne manustamine, 100 mg/kg/päevas, 28 päeva
Vaheained:
CAS nr 2031-23-4 1-(3-kloropropüül)-4-metüülpiperasiindivesinikkloriid
CAS nr 214470-66-3 7-(3-kloropropoksü)-4-hüdroksü-6-metoksükinoliin-3-karbonitriil
CAS-nr 214470-68-5 4-KLOOR-7-(3-KLOOR-PROPOKSÜ)-6-METOKSÜKINOLiin-3-KARBONITRIIL
CAS nr 263149-10-6 4-KLOOR-7-HÜDROKSÜ-6-METOKSÜKINOLIIN-3-KARBONITRIIL
CAS-nr 380844-49-5 7-(3-KLOORPROPOKSÜ)-4-(2,4-DIKLOR-5-METOKSÜ-FENÜÜLAMINO)-6-METOKSÜKINOLIIN-3-KARBONITRIIL
Toidu- ja ravimiamet (FDA) on sihipärase ravimi Bsutiniibi (Bosulif) heaks kiitnud kroonilise müelogeense leukeemia raviks. Besutiniib on kinaasi inhibiitor, mis pärsib Abl ja Src signaaliülekande radu. Ravim on ette nähtud kroonilise, kiirendatud või ägeda Philadelphia kromosoompositiivse (Ph+) CML täiskasvanud patsientide raviks, kellel on varem olnud ravimiresistentsus või talumatus, vastavalt Pfizer Oncology teadaandele. Umbes kolmandik KML-i patsientidest ei allu standardse esmavaliku ravimi Gleeveci ravile hästi, ütles Pfizer. Umbes pooled patsientidest, kellel tekib imatiniibi suhtes resistentsus või talumatus, reageerivad halvasti ka teistele teise valiku türosiinkinaasi inhibiitoritele (TKI), teatas ettevõte.
Suukaudse ravimi heakskiit põhines peamiselt I ja II faasi kliinilistel uuringutel, milles osales 500 PH-positiivset CML-i patsienti, kes ei allunud imatiniibile või kes ei talunud seda, sealhulgas erinevad rühmad kroonilises, kiirenenud ja ägedas staadiumis. Pfizeri kliinilise uuringu andmete kohaselt saavutas kolmandik varem ainult imatiniibiga ravitud patsientidest pärast 24-nädalast Bosutiniibi (500 mg üks kord päevas) võtmist tsütogeneetilise remissiooni. 27% patsientidest, kes said imatiniibi ja teist türosiinkinaasi inhibiitorit (dasatiniib, Sprycel), saavutas olulise tsütogeneetilise remissiooni. Pfizer ütles, et ravivastuse määr tõusis mõlemas rühmas pärast 24-nädalast või enamat ravimit. Pfizer märgib, et ainult 4 protsenti kroonilise haigusega patsientidest areneb pärast besutiniibi võtmist kaugelearenenud või ägedasse staadiumisse. 3.-4. astme kõrvaltoimed on trombotsütopeenia (26%), neutropeenia (11%), kõhulahtisus (9%), aneemia (9%) ja nahalööve (8%).
Bosutrise (Bosutiniib) bossutiniibi töötas algselt välja Pfizer ja see kiideti Ameerika Ühendriikides esmakordselt heaks 2012. aasta septembris kasutamiseks Ph+CML-iga täiskasvanutel, kellel on varem esinenud kroonilises, kiirenenud või ägedas staadiumis ravi resistentsust või talumatust. . BOSULIF on esimene Pfizeri ravim hematoloogiliste kasvajate raviks ja on oluline ravivõimalus Ph+CML patsientidele, kellel on varem olnud ravimiresistentsus või talumatus. Sellel laiendatud näidustusel võib olla veelgi suurem mõju kroonilise müeloidse leukeemiaga patsientide elule.
13. juulil 2020 avas India Mylan Pharmaceutical Bosutinib (Bosutinib/Bosutinib/Bosutinib) geneerilise geneerilise Bosutrise kaubandusliku müügi. Mylani Bosutrise üldine versioon maksab umbes 25% vähem kui Pfizeri originaal Bosulif. (Samuti: Pfizeri geneeriliste ravimite osakond Upjohn ühineb sel aastal Mylaniga, et luua Viatris, maailma suurim geneeriliste ravimite ettevõte, mis valmib 2020. aasta neljandas kvartalis.)




